- ซาโปนิน (Saponins)
- ซาโปนินคืออะไร
- แหล่งที่พบซาโปนิน
- โครงสร้างและคุณสมบัติของซาโปนิน
- ความเป็นพิษของซาโปนิน
- การใช้ประโยชน์ของซาโปนิน
- การประยุกต์ใช้ด้านอาหาร
- การประยุกต์ใช้ด้านเครื่องสำอาง
- การประยุกต์ใช้ด้านเภสัช /สุขภาพ
- การผลิต การสกัด และการทำให้บริสุทธิ์
- การวิเคราะห์ปริมาณซาโปนิน
- บทสรุป
- อ้างอิง
- All Pages
บทนำ
ซาโปนิน (Saponin) เป็นสารทุติยภูมิที่พบได้ทั้งในพืชและสัตว์ แต่ส่วนใหญ่พบมากในพืช คำว่า “sapon” มาจากภาษาลาตินว่า “sapo” หมายถึง สบู่ (soap) ซาโปนินเมื่อละลายน้ำจะเกิดเป็นฟองสบู่ เนื่องจากตัวมันเองมีทั้งขั้วที่ละลายในน้ำและละลายในไขมัน จึงมีคุณสมบัติเป็นผงซักฟอกธรรมชาติใช้ทำความสะอาดเสื้อผ้า พืชที่รู้จักกันทั่วไปว่าเป็นแหล่งของซาโปนินในทางการค้ามี 2 ชนิดได้แก่ Yucca schidigera จากประเทศเม็กซิโกและ Quillaja saponaria (soapbark tree) จากประเทศชิลี ซาโปนินจาก Yucca schidigera เรียกอีกอย่างว่า yucca saponin ชาวพื้นเมืองของอเมริกานิยมใช้ทำสบู่ ส่วนซาโปนินจาก Quillaja saponaria เรียกว่า quillaja saponin ในประเทศชิลีใช้เปลือกของต้น quillaja ที่มีสารซาโปนินสำหรับทำแชมพู (Saponin, 2008) พืชที่มีซาโปนินและใช้เป็นสบู่มานานและรู้จักกันทั่วไป ได้แก่ soapwort (Saponaria officinalis), soaproot (Chlorogalum pomeridianum), soapbark (Quillaja saponaria) และ soapberry (Sapindus mukorossi) ซาโปนินมีคุณสมบัติทางเคมีและกายภาพหลากหลายสามารถใช้ประโยชน์ได้หลายอย่างคือ ใช้เป็นสบู่ ยาเบื่อปลาและกำจัดหอย ตลอดจนใช้ประโยชน์ทางอุตสาหกรรม เป็นตัวทำให้เกิดฟองในอุตสาหกรรมอาหาร เช่น เครื่องดื่ม ค็อกเทลมิกซ์ คุณสมบัติลดแรงตึงผิวจึงใช้เป็นส่วนประกอบของผลิตภัณฑ์ทำความสะอาดใบหน้าและเครื่องสำอาง คุณสมบัติต้านจุลินทรีย์ (antimicrobial) และต้านเชื้อรา (anti-fungal) ใช้เป็น antinutritional factor และมีแนวโน้มที่สามารถใช้ควบคุมลูกน้ำยุงลาย (Weisman, Z. and Chapagain, BP., 2003) บางกรณีมีการใช้ในวงจำกัดเนื่องจากมีรสขม ปัจจุบันมีประโยชน์ต่อสุขภาพ เช่น ลดคอเลสเตอรอล (cholesterol) และต้านมะเร็ง (Guclu-Ustundag, O. and Mazza, G., 2007) และใช้ในรูปของยาสมุนไพร(herbal medicines) เช่น ซาโปนินจากถั่วเหลืองและกระเทียม ในเชิงพาณิชย์มีการพัฒนากระบวนการใหม่ๆ และปรับปรุงเทคโนโลยีที่มีอยู่เดิมโดยเฉพาะอย่างยิ่งการสกัด การทำให้เข้มข้น และการทำให้สารบริสุทธิ์
ซาโปนินคืออะไร
ซาโปนินเป็นสารประกอบประเภทไกลโคไซด์ (glycoside) ประกอบด้วย 2 ส่วน คือ อะไกลโคน (aglycone) และไกลโคน (glycone) ดังแสดงในรูปที่ 1 อะไกลโคนหรือจินิน (genin) เรียกอีกอย่างว่า ซาโป จินิน (sapogenin) ซึ่งเป็นสารในกลุ่มไตรเทอร์ปีนส์ (triterpenes) สเตียรอยด์ (steroids) หรือสเตียรอยด์ อัลคาลอยด์ (steroid-alkaloid) สเตียรอยด์ซาโปนินประกอบด้วยคาร์บอน 27 ตัว ส่วนไตรเทอร์ปีนส์ซาโปนินประกอบด้วยคาร์บอน 30 ตัว ส่วนที่เป็นน้ำตาลหรือที่เรียกว่า ไกลโคน (glycone) นั้นเป็นน้ำตาลโมเลกุลเดี่ยวหรือหลายโมเลกุลต่อกัน น้ำตาลส่วนใหญ่เป็น monosaccharides ได้แก่ D-glucose, D-galactose, D-glucuronic acid, D-galacturonic acid, L-rhamnose, L-arabinose, D-xylose และ D-fructose เป็นต้น ซึ่ง yucca saponin เป็นสเตียรอยด์ซาโปนิน ขณะที่ quillaja saponin เป็นไตรเทอร์ปีนส์ซาโปนิน
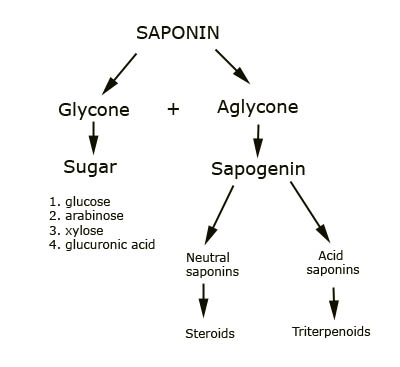
รูปที่ 1 ส่วนประกอบของซาโปนิน (saponins, 2009)
แหล่งที่พบซาโปนิน (Source of saponins)
ซาโปนินเป็นสารไกลโคไซด์ที่พบในส่วนต่างๆ ของพืช ได้แก่ ใบ ลำต้น ราก หัว ดอก และผล ในพืชวงศ์ Sapindaceae สกุล Sapindus (soapberry หรือ soapnut) และวงศ์ Aceraceae (maple) และวงศ์ Hippocastanaceae (horse chestnut) ( Saponin, 2008) ปัจจุบันมีรายงานว่าพบในพืชมากกว่า 100 วงศ์ ทั้งในพืชใบเลี้ยงเดี่ยวและคู่ พบในสัตว์ทะเลเป็นส่วนน้อย เช่น ปลาดาว แตงกวาทะเล (Sahelian, 2008) สเตียรอยด์ซาโปนินส่วนใหญ่พบในพืชใบเลี้ยงเดี่ยว เช่น วงศ์ Agavaceae, Dioscoreaceae และ Liliaceae ไตรเทอร์ปินอยด์ซาโปนินส่วนใหญ่พบในพืชใบเลี้ยงคู่ เช่น วงศ์ Leguminosae, Araliaceae และ Caryaphyllaceae เป็นต้น แหล่งของซาโปนินที่เป็นพืชอาหารพบในพืชตระกูลถั่ว เช่น ถั่วเหลือง ถั่วเขียว ถั่วปากอ้า ถั่วลิสง ถั่วเลนทิล ฯลฯ ที่พบในพืชผัก เช่น กระเทียม หน่อไม้ฝรั่ง ชา ผักโขม และมันมือเสือ ต้นสบู่ (Quillaja saponaria) มะคำดีควาย (Sapindus rarak) อัลฟัลฟา (Medicago sativa) horse chestnut (Aesculus hippocastanum) ชะเอมเทศ (Glycyrrhiza spp.) โสม (Panax spp.) ฯลฯ
ถั่วเหลืองนอกจากเป็นแหล่งของโปรตีนแล้วยังประกอบด้วยสารอื่นที่มีประโยชน์ต่อสุขภาพ เช่น ซาโปนินและไอโซฟลาโวน (isoflavone) น้ำมัน กรดไขมัน เส้นใย และสารยับยั้งทริปซิน (trypsin inhibitor) ซาโปนินและไอโซฟลาโวนเป็นสารป้องกันมะเร็งในลำไส้ใหญ่ (MacDonald, RS., et al., 2005) ลดคอเลสเตอรอลได้ กระบวนการแปรรูปถั่วเหลืองเป็นอาหารสัตว์และอาหารคนจะมีการเปลี่ยนแปลงของปริมาณซาโปนินและ ไอโซฟลาโวน พืชแต่ละชนิดมีซาโปนินเชิงซ้อนผสมรวมกัน โดยถั่วเหลืองแบ่งซาโปนินได้เป็น 3 กลุ่ม ตามโครงสร้างของอะไกลโคน คือ soyasapogenol A, B และ E ถั่วเหลืองประกอบด้วยซาโปนิน 0.1- 0.5% ในใบเลี้ยง (cotyledons) 0.2 – 0.3 % ในขณะที่ลำต้นใต้ใบเลี้ยง (hypocotyl) มีมากถึง 2 % ส่วนเปลือกที่หุ้มเมล็ดไม่พบซาโปนิน (Anderson, RL. and Wolf, WJ., 1995)
Avenacoside เป็นสเตียรอยด์ซาโปนินพบได้ในใบของข้าวโอ๊ต ส่วน avenacin เป็นไตรเทอร์ปินอยด์ซาโปนินพบในรากของข้าวโอ๊ต ซึ่งในใบอ่อนมีซาโปนินมากกว่าใบแก่ ซาโปนินในใบมีคุณสมบัติทำให้เกิดการแตกตัวของเม็ดเลือดแดงขณะปล่อยฮีโมโกลบินออกมาน้อยกว่าซาโปนินในราก ในเมล็ดถั่วเหลืองที่เพาะปลูก รากจะมี soyasapogenol A มากที่สุดขณะที่บริเวณยอดแรกเกิดมี soyasapogenol B มากที่สุด โดยทั่วไปซาโปนินที่พบในเนื้อเยื่อจะไวต่อการทำลายของเชื้อราและแบคทีเรีย รวมทั้งแมลง ดังนั้นบทบาทของซาโปนินในพืชจะทำหน้าที่เหมือนเป็นตัวขวางกั้นซึ่งเป็นระบบป้องกันตัวเองของพืช จะเห็นได้จากการพบ avenacin ปริมาณมากที่ปลายรากและพบน้อยลงในส่วนอื่นของราก โดย avenacin ทำหน้าที่เหมือนตัวควบคุมเชื้อรา Gaeumannomyces graminis อัลฟัลฟาซาโปนินเกิดจากการทำลายของแมลงซึ่งต่อมาทำหน้าที่เป็นสารไล่แมลง เมื่อใช้อัลฟัลฟาซาโปนินในอาหารสำหรับเลี้ยงตัวอ่อน Spodoptera littoralis จะช่วยยืดระยะเวลาการเปลี่ยนจากตัวอ่อนไปเป็นดักแด้ให้นานขึ้น ทำให้การเจริญเติบโตของแมลงช้าลง เพิ่มอัตราการตาย และอัตราการเกิด นอกจากนี้ซาโปนินยังสามารถควบคุมแบคทีเรียที่อยู่รอบๆ รากของพืชในดินได้ ( Wina, E., Muetzel, S., and Becker, K., 2005)
พืชชนิดเดียวกันอาจมีซาโปนินอยู่หลายชนิด เช่น ถั่วเหลืองประกอบด้วย soyasaponin A, B และ E สมุนไพรโสมประกอบด้วยจินเซ็งโนไซด์ (ginsenoside) Rb1, Rb2, Rc, Rd, Re, Rf และ Rg1 โดยตารางที่ 1 แสดงปริมาณซาโปนินที่พบในพืชซึ่งขึ้นอยู่กับชนิดพืช พันธุกรรมดั้งเดิม ส่วนต่างๆ ของพืช สิ่งแวดล้อม ปัจจัยด้านการเกษตร เช่น การเจริญเติบโตของพืช กระบวนการหรือกรรมวิธีหลังการเก็บเกี่ยวและการเก็บรักษา
ตารางที่ 1 ปริมาณซาโปนินที่พบในพืชแต่ละชนิด
|
แหล่งที่มา |
ปริมาณซาโปนิน (%) |
|
ถั่วเหลือง ถั่วหัวช้าง ถั่วเขียว Quillaja bark Yucca Fenugreek Alfalfa รากชะเอม (Licorice root) |
0.22 – 0.47 0.23 0.18 – 4.2 9 – 10 10 4 – 6 22.2 – 32.3 |
ตารางที่ 1 ปริมาณซาโปนินที่พบในพืชแต่ละชนิด (ต่อ)
|
แหล่งที่มา |
ปริมาณซาโปนิน (%) |
|
โสมอเมริกา(Pinax quinquefololium L.) ใบอ่อน ใบแก่ ราก (4 ปี) ข้าวโอ๊ต เกาลัด (Horse chestnut) ใบsugar beet Quinoa |
1.42 – 2.64 4.14 – 5.58 2.44 – 3.88 0.1 – 0.13 3 – 6 5.8 0.14 – 2.3 |
ที่มา : Guclu-Ustundag, O. and Mazza , G. (2007)
โครงสร้างและคุณสมบัติของซาโปนิน (Structure and properties of saponins)
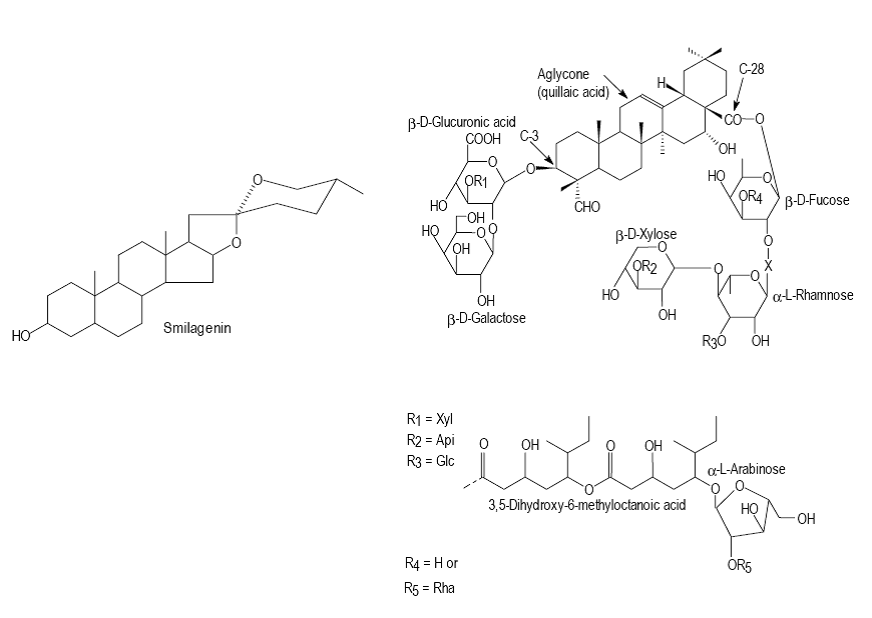
ซาโปนินแบ่งออกเป็น 2 กลุ่มตามโครงสร้างทางเคมีของอะไกลโคนคือ สเตียรอยด์ซาโปจินิน (steroidal sapogenin, C27) และไตรเทอร์ปินอยด์ซาโปจินิน (triterpenoid sapogenin, C30) ดังแสดงในรูปที่ 2 ซึ่งต่อกับโมเลกุลของน้ำตาลหนึ่งหน่วยหรือมากกว่าหนึ่งหน่วยด้วย glycosidic linkage ซาโปนินสามารถจัดเป็นกลุ่มตามจำนวนโซ่ของโมเลกุลน้ำตาลในโครงสร้างว่าเป็นmono-, di-หรือ tridesmosidic เช่น monodesmosidic saponin เป็นซาโปนินที่มีโมเลกุลของน้ำตาลหนึ่งหน่วย โดยทั่วไปจะเชื่อมกับส่วนของ sapogenin ที่คาร์บอนตำแหน่งที่สาม ส่วน didesmosidic saponin มีโมเลกุลของน้ำตาลสองหน่วยเชื่อมกับซาโปจินิน อะไกลโคนและกลุ่มที่แสดงหน้าที่ในโครงสร้างอะไกลโคน ชนิดของน้ำตาลและตำแหน่งที่เชื่อมสามารถเปลี่ยนแปลงได้จึงทำให้มีสารประกอบซาโปนินหลายกลุ่มและเนื่องจากความซับซ้อนของโครงสร้างทำให้มีคุณสมบัติทางเคมีฟิสิกส์ ดังแสดงในตารางที่ 2 (Guclu-Ustundag, O. and Mazza, G., 2007)
1. คุณสมบัติทางเคมีฟิสิกส์ (Physicochemical properties)โครงสร้างซาโปนินประกอบด้วยส่วนที่สามารถละลายได้ในไขมันหรือส่วนของอะไกลโคนและส่วนที่ละลายได้ในน้ำคือส่วนของน้ำตาล จึงทำให้เป็นสารประกอบที่มีคุณสมบัติเป็นสารซักฟอก สารเปียก ตัวกระทำอิมัลชันและทำให้เกิดฟอง เมื่ออยู่ในสารละลายสารลดแรงตึงผิวจะเกิดเป็นไมเซลล์เหนือความเข้มข้นวิกฤตเรียกจุดนี้ว่า “ความเข้มข้นขั้นวิกฤตของไมเซลล์” (critical micelle concentration, cmc) ขนาดและโครงสร้างของไมเซลล์ขึ้นอยู่กับชนิดของซาโปนินในพืช เช่น คุณสมบัติการรวมตัวเป็นไมเซลล์ของ quillaja saponin ขึ้นอยู่กับอุณหภูมิ ความเข้มข้นของเกลือและความเป็นกรด-ด่าง อุณหภูมิที่ 25 °C ค่า cmc. ของ quillaja saponin อยู่ในช่วง 0.5-0.8 กรัมต่อลิตรโดยจะเพิ่มขึ้นตามอุณหภูมิและความเป็นกรด-ด่างและลดลงตามความเข้มข้นของเกลือที่เพิ่มขึ้น การรวมตัวกันของคอเลสเตอรอลกับไมเซลล์ของซาโปนินจะเพิ่มค่า cmc ขนาด ความหนืดและจำนวนการจับตัว เป็นผลทำให้ความสามารถในการละลายของคอเลสเตอรอลมากเท่ากับ 103 เท่าที่อุณหภูมิห้อง (Guclu-Ustundag, O. and Mazza, G., 2007)นอกจากคุณสมบัติการละลายที่ขึ้นอยู่กับโครงสร้างและหมู่ที่ทำหน้าที่แล้ว ความบริสุทธิ์ของซาโปนินหรือส่วนผสมของซาโปนินก็มีผลต่อการละลายเช่นกันโดยซาโปนินชนิดหนึ่งมีผลต่อการละลายของซาโปนินอีกชนิด เช่น การละลายของ monodesmosides saponin จะเพิ่มขึ้นเมื่อมี bidesmosides saponin ผสมอยู่ด้วยและยังขึ้นกับโครงสร้างของ monodesmosides saponin เองและอัตราส่วนหรือความเข้มข้นของ bidesmosides saponin เช่น monodesmosides ของ Sapindus mukurossi ซึ่งละลายในน้ำได้น้อยจะมีการละลายเพิ่มขึ้นเมื่อมี mukurossi bidesmoside saponin
ตารางที่ 2 คุณสมบัติทางฟิสิกส์ของอะไกลโคน (Aglycone) และซาโปนิน (Saponin) บางชนิด
|
สารประกอบ |
สูตร |
การละลาย |
แหล่งที่มา |
น้ำหนักโมเลกุล |
จุดหลอมเหลว(oC) |
|
Aglycone Oleanolic acid
|
C30H48O3
|
ไม่ละลายน้ำ ละลายในอีเทอร์ 95% แอลกอฮอล์ คลอโรฟอร์ม อะซิโตน เมทานอล |
Quinoa
|
457
|
310
|
|
Quillaic acid
Diosgenin
Glycyrrhetic acid
Saponin Glycyrrhizic acid (Glycyrrhizin)
|
C30H46O5
C27H42O3
C30H46O4
C42H62O16
|
ละลายในแอลกอฮอล์ อีเทอร์ อะซิโตน เอทิลอะซิเทต กรดน้ำส้ม ละลายในตัวทำละลายอินทรีย์ทั่วไป กรดน้ำส้ม
ละลายได้ดีในน้ำร้อน แอลกอฮอล์ ไม่ละลายในอีเทอร์
|
Quillaja
Dioscorea, fenugreek, yam Licorice
Licorice
|
487
415
471
823
|
292-293
204-300
298-300
|
|
Escin a-escin
ß-escin |
|
ละลายได้ดีมากในน้ำและเมทานอล ละลายได้เล็กน้อยในอะซิโตน ไม่ละลายในอีเทอร์และไฮโดรคาร์บอนละลายได้ดีในเมทานอล ละลายได้เล็กน้อยในอะซิโตน ละลายได้น้อยมากในน้ำ ไม่ละลายในอีเทอร์และไฮโดรคาร์บอน |
Horse chestnut |
|
225-227
|
ตารางที่ 2 คุณสมบัติทางฟิสิกส์ของอะไกลโคน (Aglycone) และซาโปนิน (Saponin) บางชนิด (ต่อ)
|
สารประกอบ |
สูตร |
การละลาย |
แหล่งที่มา |
น้ำหนักโมเลกุล |
จุดหลอมเหลว(oC) |
|
Gypsophia saponin |
C35H61O24
|
ละลายในน้ำ (0.5147 กรัมต่อ 100 มิลลิลิตรที่ 25oC) |
Gypsophia |
863 |
221-227 |
ที่มา : Guclu-Ustundag, O. and Mazza , G. (2007)
ความสามารถในการละลายที่เพิ่มขึ้น มีความสำคัญต่อคุณสมบัติทางชีวภาพและกระบวนการแปรรูปซาโปนิน monodesmosides ที่บริสุทธิ์จะละลายน้ำได้น้อยมากและสามารถสกัดออกจากสารประกอบที่เกิดขึ้นร่วมกัน (co-occuring compounds)ได้ง่าย คุณสมบัติการละลายของไมเซลล์มีประโยชน์ต่อการพัฒนากระบวนการสกัดหรือมีผลต่อการละลายของส่วนประกอบในผลิตภัณฑ์เครื่องสำอาง ยาหรืออาหาร
ตัวทำละลายทั่วไปที่นิยมใช้สกัดซาโปนินคือ น้ำ แอลกอฮอล์ หรือน้ำผสมแอลกอฮอล์ โดยซาโปนินบางตัวสามารถละลายในอีเทอร์ คลอโรฟอร์ม เบนซีน เอทิลอะซิเตตและกรดน้ำส้มเข้มข้นได้ โครงสร้างที่ซับซ้อนของซาโปนินอาจมีการเปลี่ยนแปลงทางเคมีระหว่างการเก็บหรือกระบวนการแปรรูปทำให้เกิดการเปลี่ยนแปลงของคุณสมบัติต่างๆ เช่น เกิดการแยกสลายด้วยน้ำ (hydrolysis) โดยมีกรด ด่าง ความร้อนหรือ เอนไซม์เป็นตัวเร่งปฏิกิริยา เกิดเป็นอะไกลโคน โปรซาโปจินิน (prosapogenin) และน้ำตาล การละลายของอะไกลโคนจะแตกต่างจากซาโปนินเดิมอย่างมากเนื่องจากเป็นส่วนที่ละลายในไขมัน (lipophilic)
ความสัมพันธ์ระหว่างซาโปนินกับโปรตีนขึ้นอยู่กับชนิดโปรตีนและส่วนผสมซาโปนิน เช่น quillaja saponin เมื่อให้ร้อน 78°C นาน 26 นาที กับเคซิน (casein) จะเกิดเป็นสารประกอบเชิงซ้อนที่มีน้ำหนักโมเลกุลสูงในขณะที่ทำปฏิกิริยากับโปรตีนถั่วเหลืองจะเกิดการจับตัวเป็นก้อน ทั้งนี้ไม่ขึ้นกับการเติมซาโปนิน การจับตัวกันของซาโปนินและโปรตีนนี้ใช้ในการดัดแปลงคุณสมบัติของโปรตีนได้ เช่น คุณสมบัติความคงตัวต่อความร้อนและเอนไซม์
2. คุณสมบัติทางชีวภาพ (Biological activity) ซาโปนินมีคุณสมบัติทางชีวภาพมากมาย ซึ่งมีทั้งข้อดีและข้อเสีย ข้อดี เช่น เป็นสารต้านจุลินทรีย์ สารต้านอนุมูลอิสระ และลดการดูดซึมของไขมัน นอกจากนี้ ซาโปนินยังมีความเป็นพิษของต่อแมลง หนอน หอยทาก และปลา ส่วนความเป็นพิษต่อสัตว์เลือดอุ่นนั้นขึ้นอยู่กับวิธีการจัดการ แหล่งที่มา ส่วนประกอบและความเข้มข้นของส่วนผสมซาโปนิน มีคุณสมบัติทางชีวภาพที่เป็นข้อเสีย คือ ทำให้เกิดการแตกตัวของเม็ดเลือดแดง (erythrocyte) ขณะปล่อยฮีโมโกลบินออกมาเมื่อฉีดเข้าไปในร่างกายของมนุษย์ สารสกัดซาโปนินจากพืชสำหรับใช้ในการศึกษาหาฤทธิ์ทางชีวภาพเป็นแนวทางหนึ่งที่จะทราบลักษณะเฉพาะของซาโปนินหรือความสัมพันธ์ระหว่างโครงสร้างกับคุณสมบัติของซาโปนินได้ จากการศึกษาในหนูและกระต่าย พบว่า ซาโปนินจะไม่ถูกดูดซับระหว่างอยู่ในระบบทางเดินอาหารแต่จะถูกย่อยสลายเป็นซาโปจินินโดยเอนไซม์ ส่วนในคนซาโปนินจากถั่วเหลือง (soyasaponins) จะถูกดูดซึมโดยเซลล์ของลำไส้เล็กได้น้อยมากและจะถูกย่อยสลายไปเป็น soyasapogenol Bโดยจุลินทรีย์ในลำไส้เล็กแล้วถูกขับออกมาทางอุจจาระ
ซาโปนินหลายชนิดมีคุณสมบัติต้านเชื้อราที่แรงและอยู่ในพืชที่แข็งแรงสมบูรณ์โดยมีปริมาณมากทำหน้าที่เหมือนสารเคมีที่เป็นแนวป้องกันการโจมตีของเชื้อรา บางครั้งอาจจะไม่พบในพืชที่แข็งแรงสมบูรณ์แต่จะสร้างขึ้นเมื่อถูกทำลายจากแมลง โรคพืชหรือการกลายพันธุ์เพื่อเป็นการต้านเชื้อรา (Papadopoulou, K., et al., 1999)
คุณสมบัติการลดคอเลสเตอรอลในคนและสัตว์ ซาโปนินจะไปยับยั้งการดูดซึมคอเลสเตอรอลในลำไส้เล็ก หรือช่วยการดูดซึมกรดน้ำดี (bile acid) อาหารสัตว์ที่ประกอบด้วยซาโปนินบริสุทธิ์หรือซาโปนินสกัดเข้มข้น เช่น digitonin (สเตียรอยด์ซาโปนินจาก Digitalis purpurea), saikosaponin (ไตรเทอร์ปินอยด์ซาโปนินจากรากของ Bupleurum falcatum L.) และ garlic saponin ซึ่งสามารถลดคอเลสเตอรอลที่อยู่ในพลาสมาได้และลดความเข้มข้นคอเลสเตอรอลในตับ ซาโปนินและไอโซฟลาโวน (isoflavone) ในโปรตีนถั่วเหลืองสามารถช่วยลดคอเลสเตอรอลได้เช่นกัน pamaqueside และ tiqueside ซึ่งเป็นสารสังเคราะห์ที่มีโครงสร้างคล้ายซาโปนินและใช้ทดลองเพื่อลดคอเลสเตอรอลในกระต่าย พบว่า สามารถลดคอเลสเตอรอลได้ แต่มีกลไกแตกต่างไปจากซาโปนินในธรรมชาติ (Morehouse, LA., et al., 1999)
ปัจจุบันมีการศึกษาวิจัยพืชที่เป็นแหล่งของสารที่สามารถชักนำให้เซลล์ที่ผิดปรกติตายโดย Neychev, VK., et al. (2007) ได้วิจัยคุณสมบัติทางชีวภาพของซาโปนินจาก Tribulus terrestris L. ซึ่งเป็นพืชสมุนไพรในการเป็นสารต้านมะเร็ง พบว่า ซาโปนินจากพืชชนิดนี้มีความเป็นพิษน้อยต่อ fibroblasts ที่เป็นเซลล์ในผิวหนังของคนโดยเปรียบเทียบกับเซลล์มะเร็งที่ใช้ทดสอบ กลไกของโมเลกุลที่เกี่ยวข้องในการยับยั้งการแบ่งเซลล์และการชักนำให้เกิดการตายของเซลล์ โดยไตรเทอร์ปินอยด์ซาโปนินจาก Acacia victoriae (Bentham) และสาร avicins สามารถเหนี่ยวนำให้เกิดกระบวนการตายของเซลล์ (apoptosis) ได้ (Haridas, V., et al., 2001) การศึกษาความสัมพันธ์ระหว่างโครงสร้างทางเคมีกับการต้านมะเร็งในลำไส้ใหญ่ของซาโปนินจากถั่วเหลืองแสดงให้เห็นว่า soyasapogenols มีคุณสมบัติทางชีวภาพมากกว่า glycosidic saponins (MacDonald, RS., et al., 2005) dammarane saponins จากโสม กรดบิทูลินิก (betulinic acid) และกรดโอลีนโนลิก (oleanolic acid) มีคุณสมบัติต้านมะเร็งเช่นกัน นอกจากนี้ oleanolic acid ยังมีคุณสมบัติต้านไวรัส (HIV) ต้านการอักเสบ ต้านการเกิดแผลพุพอง ป้องกันตับอักเสบและต้านแบคทีเรีย
การเปลี่ยนซาโปนินให้เป็นอะไกลโคนมีผลทำให้สูญเสียคุณสมบัติทางชีวภาพได้ เช่น การย่อยสลายซาโปนินโดยแบคทีเรียในกระเพาะสัตว์เคี้ยวเอื้องมีผลเสียต่อการทำงานของโปรโตซัว ทำนองเดียวกันการเอาหมู่เอซิลออก (deacylation) จาก quillaja saponin จะลดความสามารถในการเป็นสารปรุงแต่ง (additive)
ซาโปนินจากชาได้จากเมล็ดชาเป็นแหล่งซาโปนินใหม่ของประเทศจีน ซาโปนินจากใบชามีคุณสมบัติต้านอาการแพ้ ซาโปนินจากเมล็ดชานิยมใช้ในการทำความสะอาดบ่อเลี้ยงปลาและกุ้ง เพื่อกำจัดศัตรูที่เป็นอันตรายแก่สัตว์เลี้ยงในบ่อ อีกทั้งซาโปนินจากชายังมีคุณสมบัติเป็นสารกำจัดศัตรูพืชที่ใช้กำจัดแมลงและโรคพืช (Wina, E., et al., 2005)
ความเป็นพิษของซาโปนิน (Toxicity of saponins)
ซาโปนินมีความเป็นพิษสูงต่อสัตว์เลือดเย็น เช่น ปลา หอย กบ และสัตว์ที่หายใจด้วยเหงือก โดยทำให้เกิดอัมพาต (paralysis) ที่เหงือก จึงนำมาใช้เป็นยาเบื่อปลาได้ เช่น ส่วนของ sapogenin aglycone ที่พบในพิษงู ปลาดาวและแตงกวาทะเล ซาโปนินบางชนิดรวมทั้งซาโปนินจาก soapberry มีความเป็นพิษถ้ากลืนเข้าไปและเป็นสาเหตุของผื่นคันที่ผิวหนังได้ ซาโปนินที่เป็นพิษเรียกว่า sapotoxin ซึ่งซาโปนินจาก Digitalis ถูกนำมาใช้เป็นสารพิษอาบหัวลูกศรและหอกของชาวพื้นเมืองแอฟริกาและอเมริกาใต้ นอกจากนี้ซาโปนินยังมีความเป็นพิษสูงถ้าถูกฉีดเข้าในร่างกายเนื่องจากทำให้เกิดการแตกตัวของเม็ดเลือดแดง (erythrocyte) ขณะปล่อยฮีโมโกลบินออกมา ซาโปนินสามารถแยกสลายด้วยน้ำ (hydrolysis) เป็นน้ำตาลและอะไกลโคนหรือซาโปจินินได้เมื่อกลืนเข้าไปในร่างกาย ทำให้ความเป็นพิษของซาโปนินลดลง แต่บางคนก็อาจเกิดผื่นคันบริเวณผิวหนังได้ ชาวพื้นเมืองอเมริการับประทานไอศกรีมที่ทำจาก Canada Buffaloberry ซึ่งมีซาโปจินินอยู่และอาหารสุนัขที่มีถั่วเหลืองและหัวบีทเป็นส่วนประกอบในอาหารอาจเป็นพิษต่อสุนัขได้ (Saponins, 2008) ความเป็นพิษของกรด glycyrrhizic ในชะเอมมีผลทำให้มิเนอราลคอร์ติคอยด์ (mineralcorticoid) ซึ่งเป็นฮอร์โมนที่สร้างจากอะดรีนัลคอร์เทกซ์ของต่อมหมวกไต (mineralcorticoid activity) ทำงานเพิ่มขึ้น ทำให้เกิดความไม่สมดุลของแร่ธาตุในร่างกายเนื่องจากเกิดการตกค้างของโซเดียม (sodium retention) และการขับโพแตสเซียม (potassium excretion) ออกจากร่างกาย รวมทั้งน้ำในร่างกายเป็นผลให้เกิดความดันโลหิตสูงตามมา (Guclu-Ustundag, O. and Mazza, G., 2007)
การใช้ประโยชน์ของซาโปนิน (Application of saponins)
จากคุณสมบัติทางเคมีฟิสิกส์และทางชีวภาพที่มีความหลากหลายของซาโปนิน จึงมีการประยุกต์ใช้ ซาโปนินในเชิงพาณิชย์ เช่น อาหารคนและสัตว์ เครื่องสำอาง ผลิตภัณฑ์ทางการเกษตรและเภสัชกรรม ซึ่งปัจจุบันมีแนวโน้มในการใช้สารธรรมชาติเป็นองค์ประกอบเพื่อเพิ่มคุณสมบัติทางชีวภาพ จึงทำให้มีความต้องการซาโปนินเพิ่มขึ้น เนื่องจากคุณสมบัติการลดแรงตึงผิวที่ไม่มีประจุ จึงนิยมใช้ซาโปนินเป็นอิมัลซิไฟเออร์ สารทำให้เกิดฟอง (foaming agents) และสารซักฟอก (detergents) นอกจากนี้ยังใช้เป็นสารปรุงแต่งในอาหารสัตว์ สารกระตุ้นการเจริญเติบโตของพืชและรักษาฟื้นฟูสภาพดิน แหล่งของซาโปนินที่ใช้ทางการค้าคือ ซาโปนินที่สกัดจาก Quillaja saponaria และ Yucca schidigera และซาโปนินที่สกัดจากพืชชนิดอื่นได้แก่ horse chestnut และถั่วเหลือง นำมาใช้ทางเภสัชกรรมเป็นวัตถุดิบในการผลิตฮอร์โมน การศึกษาภูมิคุ้มกันและเป็นส่วนประกอบของผลิตภัณฑ์เกี่ยวกับสุขภาพ เช่น สารสกัดจากสมุนไพรต่างๆ และมีการเพิ่มมูลค่าของผลิตผลพลอยได้จากการสกัดซาโปนินในพืช เช่น สารตกค้างจากการสกัดน้ำมันถั่วเหลือง กากน้ำตาลจากถั่วเหลืองและของเหลือทิ้งจากหน่อไม้ฝรั่ง
ซาโปนินที่เกิดสารประกอบเชิงซ้อนเป็นไมเซลล์ร่วมกับสเตอรอล เช่น คอเลสเตอรอลและกรดน้ำดีถูกนำมาใช้แยกคอเลสเตอรอลออกจากผลิตภัณฑ์นม เช่น น้ำมันเนย (butter oil) ซึ่งปฏิกิริยาระหว่างซาโปนินกับเยื่อหุ้มเซลล์สามารถเกิดการตกตะกอนกับไขมันที่เยื่อหุ้มเซลล์ของหางนมภายหลังที่ทำเนยแล้วได้ ซาโปนินยังนำมาใช้เพิ่มคุณสมบัติการไม่ชอบน้ำของเยื่อหุ้มเซลล์ของไขมันเพื่อช่วยในการจับกลุ่มและตกตะกอนเป็นสารประกอบเชิงซ้อน (Guclu-Ustundag, O. and Mazza, G., 2007) นอกจากนี้ซาโปนินจากใบหรือเมล็ดของพืชตระกูลถั่วใช้เป็นอาหารหรือสารเติมแต่งในอาหารของสัตว์เคี้ยวเอื้อง เช่น ปัจจุบันมีการใช้ซาโปนินที่สกัดจาก yucca (yucca saponin) และ quillaja (quillaja saponin) ในอาหารสัตว์และคนโดย yucca saponin ใช้เป็นสารเติมแต่งในอาหารสัตว์เพื่อลดกลิ่นแอมโมเนียและกลิ่นมูลสัตว์ ในสัตว์เคี้ยวเอื้องซาโปนินมีคุณสมบัติต้านการทำงานของโปรโตซัวโดยเกิดสารประกอบเชิงซ้อนร่วมกับคอเลสเตอรอลในโปรโตซัวและยับยั้งการทำงานของแบคทีเรียบางชนิดในกระเพาะ ทำให้แอมโมเนียเกิดน้อยลง yucca saponin ยังใช้ป้องกันและรักษาโรคไขข้ออักเสบในม้าและซาโปนินยังช่วยการดูดซึมไขมันโดยเกิดเป็นไมเซลล์ร่วมกับเกลือน้ำดี (bile salts) ทำให้คอเลสเตอรอลในลำไส้เล็กลดลง ส่วน quillaja saponin ถูกใช้เป็นสารเติมแต่งในวัคซีนสัตว์ เพื่อเพิ่มความต้านเชื้อโรคโดยการฉีด ซึ่งซาโปนินจะมีผลต่อระบบเยื่อหุ้มเซลล์ (Cheeke, RP., 2000)
การประยุกต์ใช้ด้านเภสัช /สุขภาพ (Pharmaceutical/Health applications)
การผลิต การสกัด และการทำให้บริสุทธิ์ (Production, extraction and purification)
การประยุกต์ใช้ซาโปนินในด้านอาหาร ยาและเครื่องสำอางเป็นอย่างมากนั้น จึงทำให้มีการผลิตซาโปนินในเชิงพาณิชย์หรือระดับการค้า จากที่กล่าวมาแล้วว่าโมเลกุลของซาโปนินประกอบด้วยอะไกลโคนและน้ำตาล ซึ่งน้ำตาลอาจเป็นตัวเดียวหรือเป็นโซ่ของน้ำตาลต่อกันสองหรือสามหรือมากกว่าขึ้นไปในส่วน อะไกลโคนเป็นกลุ่มของสเตียรอยด์หรือไตรเทอร์ปีนส์ที่มีหมู่ฟังก์ชัน เช่น ไฮดรอกซิล (hydroxyl, -OH), คาร์บอกซิล (carboxyl, -COOH), เมธิล (methyl, -CH3) อยู่ในโครงสร้างในตำแหน่งที่แตกต่างกันไป ดังนั้นซาโปนินจึงมีมากมายหลายชนิดในพืช ในพืชชนิดเดียวกันชนิดและปริมาณของซาโปนินจะต่างกันในแต่ละส่วนของพืช ความหลากหลายของโครงสร้างนี้ทำให้ซาโปนินมีความเป็นขั้วในช่วงกว้าง ซึ่งยากต่อการแยกและหาปริมาณ ซาโปนินแต่ละชนิด
ความสามารถในการเกิดฟองได้นานของซาโปนินถูกใช้ในการตรวจหาซาโปนินในพืชโดยมีข้อเสียคือถ้าในโมเลกุลของซาโปนินต่อกับโซ่น้ำตาล 2-3 ตัว การเกิดฟองจะไม่คงทนหรือสารสกัดจากพืชบางชนิดที่ไม่มีซาโปนินอาจทำให้เกิดฟอง ซึ่งทำให้มีการเข้าใจผิดได้ ซาโปนินบางชนิดที่ทำให้เกิดการแตกตัวของเม็ดเลือดแดง (erythrocyte) ขณะปล่อยฮีโมโกลบินออกมาอาจใช้วิธีกึ่งการตรวจหาปริมาณ ซึ่งขึ้นอยู่กับโครงสร้างและวิธีที่ใช้ (Oleszek, WA., 2002) ซาโปนินที่มีโครงสร้างเป็นน้ำตาลโมเลกุลเดี่ยวจะทำให้การแตกตัวของเม็ดเลือดแดง (erythrocyte) ขณะปล่อยฮีโมโกลบินออกมาดีกว่าซาโปนินที่มีโมเลกุลของน้ำตาลเกาะสองหน่วยและการหาปริมาณซาโปนินในพืชโดยวิธีดั้งเดิมจะใช้วิธีการชั่งน้ำหนัก (gravimetric method) วิธีทางชีวภาพเป็นวิธีที่ไม่ยุ่งยากแต่เป็นการคาดประมาณที่ไม่สามารถบอกความแตกต่างของซาโปนินแต่ละชนิดได้ เหมาะสำหรับการหาปริมาณซาโปนินทั้งหมด ซึ่งต้องมีการทำมาตรฐานของซาโปนินแต่ละชนิดที่ได้จากพืชนั้นๆ เนื่องจากคุณสมบัติทางชีวภาพมีความสัมพันธ์โดยตรงกับโครงสร้างทางเคมีของซาโปนินแต่ละตัวและความเข้มข้นอาจเปลี่ยนแปลงได้ขึ้นอยู่กับปัจจัยหลายอย่าง เช่น อายุของพืช ระยะการเจริญเติบโต ลักษณะของสิ่งแวดล้อมและองค์ประกอบของสารสกัดซาโปนินจากพืช ซึ่งมีความสำคัญและเกี่ยวข้องกับความถูกต้องในการเตรียมตัวอย่างและมีผลต่อการตรวจวิเคราะห์ของวิธีทางชีวภาพ
วิธีอื่นๆได้แก่ วิธีสเปกโตรโฟโตเมตริก TLC-densitometry, gas chromatography (GC), high performance liquid chromatography (HPLC), LC-MS, LC-NMR และ capillary electrophoresis (CE) ซึ่งวิธี TLC-densitometry, gas chromatography (GC) และ high performance liquid chromatography (HPLC) เป็นวิธีที่ใช้หาปริมาณของ sapogenins และ/หรือซาโปนินในพืช ส่วนวิธี LC-MS และ LC-NMR เป็นเทคนิคในการคัดกรองซาโปนินในสารสกัดหยาบจากพืชและเป็นวิธีที่ดีสำหรับการตรวจหาสารใหม่ที่มีศักยภาพทางชีวภาพโดยไม่จำเป็นต้องสกัดสารออกมา (Oleszek, WA., 2002)
คาร์บอนไดออกไซด์ยิ่งยวด (Supercritical CO2) เป็นทางเลือกหนึ่งที่ทดแทนตัวทำละลายอินทรีย์สำหรับการสกัดสารธรรมชาติซึ่งมีข้อดีในการเอาตัวทำละลายออกและผลิตภัณฑ์ที่ได้ปราศจากตัวทำละลาย เช่น การสกัด ginsenosides จากโสม saikosaponins จาก Bupleurum chinense และ glycyrrhizic acid จากชะเอมเทศ (Guclu-Ustundag, O., and Mazza, G., 2007)
3. การทำให้ซาโปนินบริสุทธิ์ (Purification of saponins) การทำให้สารสกัดหยาบของซาโปนิน บริสุทธิ์ เป็นขั้นตอนหลังจากการสกัดซาโปนินออกจากพืชแล้วเกี่ยวข้องกับการการแบ่งส่วน (partition) ของสารสกัดหยาบซาโปนินระหว่างน้ำกับตัวทำละลายที่ไม่รวมตัวกับน้ำ เช่น n-butanol และขั้นตอนต่อจากการแบ่งส่วนคือ การตกตะกอน การดูดซับ การกรองโดยใช้เมมเบรนชนิด ultrafiltration และวิธีโครมาโตกราฟี ซึ่งวิธีโครมาโตกราฟีเป็นวิธีที่ใช้กันอย่างกว้างขวางโดยสามารถวิเคราะห์ปริมาณได้ด้วย (Guclu-Ustundag, O. and Mazza, G., 2007) กระบวนการที่ได้สิทธิบัตรแล้วในการสกัดแยกซาโนนินจากถั่วเหลืองและผลิตภัณฑ์จากถั่วเหลืองด้วยส่วนผสมของตัวทำละลายระหว่างอะซิโตนและน้ำในอัตราส่วนและอุณหภูมิต่างๆ เพื่อประหยัดค่าใช้จ่ายและได้ซาโปนินจากถั่วเหลืองที่มีความบริสุทธิ์สูง ในขณะเดียวกันก็ได้ไอโซฟลาโวนเป็นผลพลอยได้ด้วย โดยการใช้อัตราส่วนของอะซิโตนต่อน้ำที่เหมาะสมที่สุดคือ 4:1 โดยน้ำหนัก จากนั้นแยกซาโปนินออกมาด้วยการกรองหรือการหมุนเหวี่ยงหรือทิ้งให้ตกตะกอนในอะซิโตนที่เย็นซึ่งจะได้ซาโปนินที่บริสุทธิ์มากกว่า 70% (Wiley Organic, Inc., 2002)
การวิเคราะห์ปริมาณซาโปนิน (Quantitative analysis of saponins)
วิธีทางโครมาโตกราฟีเป็นวิธีที่ดีสำหรับแยกซาโปนินแต่ละชนิดเพื่อตรวจหาปริมาณของซาโปนินจะใช้ควบคู่กับการตรวจวัดด้วยวิธีสเปกโตรโฟโตเมตริก (spectrophotometric method) และวิธีทางชีวภาพ (biological method) ซึ่งวิธีทางชีวภาพและสเปกโตรโฟโตเมตริกก็ไม่สามารถให้ข้อมูลที่ถูกต้องเนื่องจากโครงสร้างของซาโปนินมีความหลากหลายจึงมีวิธีดีกว่าดังนี้ คือ
1. Thin-layer chromatography-Densitometer (TLC-densitometer) เป็นเทคนิคที่ใช้ในการแยกและตรวจหาซาโปนินที่สกัดจากพืชหลายชนิด โดยการวัดความหนาแน่น (Densitometry) ปัญหาหลักของวิธีนี้คือ ต้องทำสารมาตรฐานควบคู่ไปกับตัวอย่างในทุกแผ่นTLC เพื่อลดความแปรผันระหว่างแผ่นและสีที่เกิดปฏิกิริยาจากสารที่ใช้พ่น (spraying reagent) อีกทั้งการตรวจวัดจุดหรือตำแหน่งของสารต้องใช้ซอฟแวร์ที่มีความไวสูงในการสแกน แผ่นกระจกที่เคลือบด้วยซิลิกาเจลซึ่งถูกเป็นส่วนที่อยู่นิ่ง (stationary phase) ในการแยกส่วนที่เคลื่อน (mobile phase) หรือ developing system ประกอบด้วยส่วนผสมของ chloroform-methanol-water หรือ butanol-acetic acid-water สำหรับวิเคราะห์ซาโปนินและ benzene-acetone สำหรับวิเคราะห์อะไกลโคน spraying reagent ที่ใช้ ได้แก่ phosphotungstic acid, 10% sulfuric acid ใน ethanol และ 0.5% p-anisaldehyde 1% sulfuric acid ใน acetic acid ความสัมพันธ์เชิงเส้นระหว่าง peak area และปริมาณสารมาตรฐานของซาโปนินพบว่าอยู่ในช่วง 1-5 ไมโครกรัมต่อจุดโดยมีค่า recovery 98% ค่าเบี่ยงเบนมาตรฐาน 3-5% เมื่อเปรียบเทียบกับวิธี HPLC พบว่า เป็นวิธีที่ถูกต้องเพียงพอสำหรับการเฝ้าระวังและควบคุมคุณภาพและเหมาะสำหรับการตรวจเป็นชุด 2D-TLC สามารถใช้ตรวจสารสกัดซาโปนินได้ 35 ชนิดจากต้น ใบโสมและซาโปนินจาก Calendula officinalis เทคนิคนี้ยังใช้ตรวจหา glycyrrhizic acid ในสารสกัดจากชะเอมเทศ panaxadiol และ panaxatriol ในโสมและซาโปนินจาก Avena sativa วิธีนี้สามารถใช้ตรวจตัวอย่างได้เป็นจำนวนมากโดยไม่ต้องมีการทำความสะอาดตัวอย่างก่อนการวิเคราะห์ จึงเป็นวิธีที่แนะนำสำหรับการควบคุมคุณภาพของยาที่ดี (Oleszek, WA., 2002)
2. TLC-colorimetry การวิเคราะห์ซาโปนินทางคุณภาพและปริมาณสามารถทำด้วยการวัดสี โดย ซาโปนินแต่ละชนิดจะถูกแยกออกเป็นแถบสีด้วยเทคนิค TLC แถบเหล่านี้จะถูกสกัดเอาซาโปนินออกด้วยแอลกอฮอล์ สารสกัดที่ได้จะนำไปทำปฏิกิริยากับรีเอเจนต์ตัวอื่นเพื่อทำให้เกิดสี ได้แก่ Ehrlich หรือ vanilla reagent และวัดสีที่ความยาวคลื่น 515- 560 nm ข้อเสียของวิธีนี้คือ สารบางตัวที่อยู่ในสารสกัด เช่น sterol และกรดน้ำดีที่มีหมู่ไฮดรอกซิล(OH) ที่ตำแหน่ง C-3 อาจเกิดสีกับรีเอเจนต์ได้ทำให้การวิเคราะห์ไม่ถูกต้อง anisaldehyde-sulfuric acid-ethyl acetate reagent สามารถเกิดสีกับสเตียรอยด์ซาโปจินินโดยไม่ถูกรบกวนจากสารอื่นและอาจใช้ reverse-phase cleanup ก่อนการวิเคราะห์ด้วยวิธีนี้เพื่อปรับปรุงให้มีประสิทธิภาพเพิ่ม ทั้งนี้ขึ้นกับธรรมชาติของซาโปนินด้วย (Oleszek, WA., 2002)
5. Capillary electrophoresis (CE) เป็นเทคนิคที่เหมาะสมสำหรับการแยกและหาปริมาณของสารพฤกษเคมี (phytochemicals) ที่หลากหลายในพืช โดยใช้เวลาในการแยกเร็ว (1-30 นาที) ใช้ตัวอย่างน้อยมาก (นาโนลิตร) และใช้รีเอเจนต์ที่เข้าทำปฏิกิริยาน้อยเมื่อเทียบกับวิธีอื่นๆ แต่การใช้ปริมาณตัวอย่างน้อยและความเข้มข้นสูงเพื่อทำการตรวจวัดถือเป็นข้อจำกัดของวิธีนี้ ทำให้วิธีนี้ยังไม่แพร่หลายเท่าที่ควร การทดลองใช้วิธี CE พบว่า ความเข้มข้นของบัฟเฟอร์ (นิยมใช้บอเรต) และอุณหภูมิที่เหมาะสมคือ 150 มิลลิโมลและที่อุณหภูมิห้อง ตามลำดับ (Oleszek, WA., 2002)
บทสรุป
ซาโปนินเป็นสารประกอบที่มีอยู่ในพืชหลากหลายชนิด มีโครงสร้างประกอบด้วย 2 ส่วนคือ ส่วนที่เรียกว่า อะไกลโคน (aglycone) หรือ ซาโปจินิน (sapogenins) ซึ่งมีหมู่ฟังก์ชัน (functional group) แบบต่างๆ และส่วนไกลโคน (glycone) หรือส่วนที่เป็นน้ำตาล ซึ่งอาจเป็นน้ำตาลหนึ่งหน่วยหรือมากกว่าหนึ่งหน่วยซาโป จินินเป็นสารในกลุ่มไตรเทอร์ปีนส์ (C30), สเตียรอยด์ (C27) หรือสเตียรอยด์อัลคาลอยด์ (มีอะตอมของไนโตรเจนอยู่ในโครงสร้าง) จากโครงสร้างที่ซับซ้อนจึงทำให้มีคุณสมบัติทางเคมีฟิสิกส์และทางชีวภาพหลากหลายและมีการประยุกต์ใช้ในเชิงพาณิชย์มากมาย เช่น ในอาหาร เครื่องสำอาง การเกษตรและเภสัชกรรม ตลาดปัจจุบันมีแนวโน้มที่จะใช้สารสกัดจากธรรมชาติเป็นองค์ประกอบในผลิตภัณฑ์ที่เกี่ยวข้องกับสุขภาพมากขึ้น ทำให้ความต้องการซาโปนินเพิ่มขึ้นตามไปด้วย ดังนั้นคุณภาพและปริมาณของซาโปนินในวัตถุดิบและปัจจัยที่เกี่ยวข้องกับการสกัดซาโปนินจึงมีความสำคัญต่อกระบวนการผลิต และการนำไปใช้ประโยชน์เป็นอย่างมาก
อ้างอิง
Anderson, RL., and Wolf, WJ. Compositional changes in trypsin inhibitors, phytic acid, saponins and isoflavones related to soybean processing.
The Journal of Nutrition, 1995, vol. 125, no.3, p. 581S-588S.
Cheeke, PR. Actual and potential applications of Yucca schidigera and Quillaja saponaria saponins in human and animal nutrition.
Journal of Animal Science, 2000, vol. 77, p. 1-10.
Chengdu Di’Ao Pharmaceutical Group Co., Ltd. Pharmaceutical composition containing steroidal saponins, the preparation method and use thereof.
Int.Cl. A61K 31/70 A61P 9/06 A61P 9/10. US. Patent Application Publication. US 2007/0254847 A1 2007-11-01.
Guclu-Ustundag, O. and Mazza, G. Saponins: properties, applications and processing. Critical Reviews in Foods Science and Nutrition, 2007,
vol. 47, p. 231-258.
Haridas, V., et al. Avicins:Triterpinoid saponins from Acacia victoriae (Bentham) induce apoptosis by mitochondrial perturbation. PNAS, 2001,
vol. 98, no. 10, p. 5821-5826.
Kim, JH., Chang, EJ., and Oh, HI. Saponin production in submerged adventitious root culture of Panax ginseng as affected by culture conditions and elicitors.
Asia Pacific Journal of Molecular Biology and Biotechnology, 2005, vol. 13, no. 2, p. 87-91.
LVMH Recherche,. Cosmetic or dermatologocal composition containing at least one saponin of the ginsenoside type, and its applications, especially for
treating the hair. Meybeck, A. and Bonte, F. Int.Cl. A61K 31/56. US. Pat. 5,663,160. 1997-09-02.
MacDonald, RS., et al. Environmental influence on isoflavones and saponins in soybeans and their role in colon cancer. The Journal of Nutrition, 2005,
vol. 135, no. 5, p. 1239-1242.
Morehouse, LA., et al. Comparision of synthetic saponin cholesterol absorption inhibitors in rabbits: evidence for a non-stoichiometric, intestinal mechanism
of action. Journal of Lipid Research, 1999, vol. 40, p. 464-474.
Neychev, VK., et al. Saponins from Tribulus terrestris L. are less toxic for normal human fribroblasts than for many cancer lines: influence on apoptosis
and proliferation. Experimental Biology and Medicine, 2007, vol. 232, p. 126-133.
Oleszek, WA. Chromatographic determination of plant saponins. Journal Chromatography A, 2002, vol. 967, p. 147-162.
Olmstead, MJ, et al. Organic toothpaste containing saponin. Int. Cl. A61K7/16 US. Pat. 6,485,711 B1. 2002-11-26.
Papadopoulou, K., et al. Compromised disease resisteance in saponin-deficient plants. PNAS, 1999, vol. 96, no. 22, p. 12923-12928.
Sahelian, R. Saponin. [Online][Cited 4 June 2008] Available from internet: http://www.raysahelian.com/saponin.html
Saponin. [Online][Cited 4 June 2008] Available from internet: http://en.wikipedia.org/wiki/Saponins
Wiley Organic, Inc. A process for isolating saponins from soybean-derived materials. Bobbins, T. C07H 15/00. WO. WO 02/055529 A2. 2002-07-18.
Wina, E., Muetzel, S., and Becker, K. The impact of saponins or saponin-containing plant materials on ruminant production-a review.
J. Agric. Food Chem, 2005, vol. 53, p. 8093-8105.
